Рождение первого гальванического элемента было связано с именем Вольта. Первым элементом был вольтов столб.
На одной из витрин под стеклом было выставлено письмо Вольта президенту лондонского Королевского общества Бенксу от 20 марта 1800 года. Письмо испещрено было сделанными Вольта рисунками, поясняющими устройство его удивительного прибора—вольтова столба.
Тут же были помещены рисунки первого чашечного, или стаканного, элемента Вольта.
Этот первый элемент оказался малопригодным для использования в длительной работе. Цинк, соединяясь с кислотой, вытеснял из нее водород. Пузырьки этого газа покршвали пластинки и препятствовали дальнейшему течению электричества. Это явление назвали поляризацией элемента.
Тридцать пять лет велась ожесточенная борьба ученых и изобретателей с вредным явлением поляризации. Десятки ухищрений придумывали химики, чтобы избавиться от нее.
Знаменитый французский физик Антуан Беккерель ближе всех подошел к решению этой задачи. Он предложил опускать пластинки в разные растворы, причем выделяющийся водород должен химически соединяться с одним из растворов.
За эту мысль Беккереля ухватились многие изобретатели. Одному из них удалось добиться особенного успеха, фамилия его Даниэль. Шесть лет прошло в упорном труде, прежде чем Даниэль сконструировал первый элемент, не подвергающийся поляризации. Успеху Даниэля способствовали знание химии и опыт в конструировании химических приборов. С 1831 года он был профессором химии лондонского Королевского колледжа.
Гальванический Элемент Даниэля сделан следующим образом. В глиняный цилиндр наливается раствор серной кислоты, и в нее погружается цинковый цилиндр. Пространство между стенками глиняного цилиндра и внешнего, стеклянного сосуда заполняется раствором медного купороса, в который погружается медный цилиндр. Образующийся при растворении цинка водород проходит через поры глиняного сосуда, вытесняет медь из раствора медного купороса и образует серную кислоту, в то время как вытесненная медь выделяется на медном цилиндре. Убыль меди в растворе пополняется разложением положенных на дно сосуда кристаллов медного купороса.
Но вскоре выяснилось, что элемент Даниэля обладает существенным недостатком: электродвижущая сила его мала; она не превышает 1,1 вольта. Часть электрической энергии тратится в самом элементе на разложение медного купороса.
Английский химик Вильям Грове в 1840 году решил вместо раствора медного купороса применить азотную кислоту, заменив медную пластинку платиновой.
Когда был изготовлен элемент Грове, оказалось, что предположения изобретателя оправдались: электродвижущая сила элемента Грове достигла 1,65 вольта. Оставалось лишь найти вещество, могущее заменить в элементе дорогостоящую платину.
Эту задачу в 1842 году решил знаменитый химик Роберт Бунзен, Вместо платины Бунзен применил в своем элементе очень плотно спрессованный древесный' уголь. Действие такого элемента проявилось еще сильнее: электродвижущая сила достигла 1,8 вольта. Но и этот элемент не лишен был недостатков: азотная кислота выделяла удушливые пары; трудно было находиться вблизи работающего элемента. Началась новая полоса исканий и усовершенствований.
В 1843 году женевский физик Август Делариз высказал оригинальную мысль, как избавиться от действия поляризации. Он предложил ввести в элемент в качестве деполяризатора перекись марганца, вещество, очень богатое кислородом. Так как водород жадно стремится соединиться с кислородом,, будут достигнуты наилучшие условия работы элемента. Но прошло двадцать пять лет, прежде чем впервые эта идея была осуществлена талантливым парижским химиком Георгом Лекланше. Это произошло в 1868 год£.
Глиняная пористая банка заполнялась смесью перекиси марганца с кусочками плотного угля, и сюда же вставлялся угольный электрод. Этот пористый сосуд ставился в стеклянный, заполненный раствором нашатыря (хлористого аммония). Сюда же вставлялся цинковый электрод. Элемент Лекланше развивает свою полную энергию в течение короткого времени и затем должен несколько «передохнуть», так как деполяризация в нем совершается довольно медленно. Учитывая эти свойства, элемент Лекланше применяют лишь там, где не требуется непрерывная работа (например, для электрических звонков в квартирах).
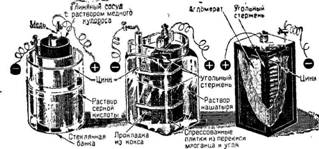
Современные гальванические элементы. Слева — элемент Даниэля, в середине — Лекланше, справа — сухой элемент»
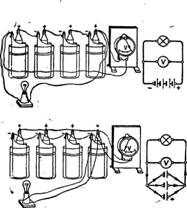
Схемы соединения элементов. Наверху—последовательное соединие, внизу—параллельное.
Огромный интерес публики вызвал оригинальный «элемент горения» талантливого русского инженера П. Н. Яблочкова. В этом элементе электричество возникало в процессе соприкосновения водяного пара с раскаленным углем. Яблочков указывал, что «элемент горения» может развить неслыханную мощность до 30 квт, т. е. в 100 раз бльшую, чем во всяком другом элементе. Но сам изобретатель считал работу над элементом еще не законченной. И после Яблочкова никто его опытов не продолжал.
«Открытие и усовершенствование вторичных элементов»—такую надпись можно было прочесть над следующими витринами Парижской выставки.
Здесь была показана история электрических аккумуляторов. Так стали называться гальванические элементы, обладающие способностью накоплять электрическую энергию при зарядке их током от другого источника и затем возвращать ее во время работы.
В середине XIX века у известного парижского. физика Александра Беккереля — сына Антуана — работал в качестве ассистента молодой ученый Гастон Плантэ. Эта фамилия была хорошо известна парижанам. Брат Гастона был выдающимся пианистом. Эту же фамилию вскоре в еще большей степени прославил Гастон своим бессмертным изобретением.
Плантэ очень тщательно исследовал процессы, происходящие в свинцовом элементе, и вот к каким выводам он пришел.
Если погрузить две покрытые окисью свинцовые пластины в сосуд с раствором серной кислоты и пропустить через них гальванический ток, то на каждую из пластин он воздействует по-разному. Та пластина, которая присоединена к отрицательному полюсу (катод), окажется покрытой водородом, выделяющимся при разложении током серией кислоты. На положительной свинцовой пластине (анод) выделится кислород. Эта положительная пластина, соединяясь с кислородом, образует перекись свинца и становится темно-коричневой. Отрицательная пластина становится все более металлически чистой. Окружающий ее водород жадно отнимает у свинца кислород, и пластина все более раскисляется.
По прошествии некоторого времени у каждой из пластчн замечается выделение пузырьков газа. Это свидетельствует о том, что процесс зарядки аккумулятора окончен. При соединении обоих электродов проводником по нему проходит ток, обратный первоначальному направлению. По прошествии некоторого времени обе пластины делаются опять химически однородными и в одинаковой мере покрытыми окисью свинца. Чтобы вновь сделать элемент пригодным к действию, необходимо опять зарядить его.
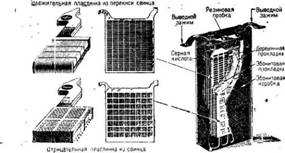
Устройство современного кислотного аккумулятора.
8 февраля 1881 года ученик Плантэ Камилл Фор запатентовал новый способ, ускоряющий формование аккумуляторов. Фор предложил заранее наносить на пластины слой свинцового сурика. Когда оценили изобретение Фора, на аккумуляторы появился огромный спрос. Новые источники электрической энергии—электрические машины постоянного тока—значительно усилили его. Аккумуляторы применялись в помощь работающим машинам, когда их энергии не хватало. Это происходило обычно утром и вечером, когда была очень большая потребность в электрической энергии. Гораздо, дешевле устроить аккумуляторные батареи и их энергией покрывать, временный недостаток, нежели устанавливать дополнительные дорогостоящие машины: в ночные часы аккумуляторы могли забирать для своей зарядки излишки имеющейся энергии и утром их возвращать.
Пятьдесят тысяч различных опытов произвел гениальный изобретатель Эдисон и создал свой тип—железо-никелевый щелочной аккумулятор. Большое распространение получили также аккумуляторы бельгийских электриков братьев Тюдор.
Так в течение целого столетия, начиная с первых элементов Вольта, многочисленные ученые и изобретатели занимались поисками наилучшего элемента, то есть такого источника тока, который действовал бы устойчиво и безотказно.